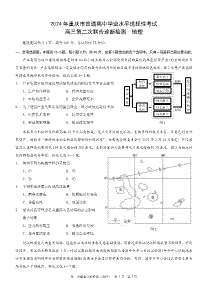
绝密★启用前A.用装置甲制取Cl2B.用装置乙除去Cl2中少量HCl2024届高三12月大联考考后强化卷(河北卷)C.用装置丙分离MnO2和MnCl2溶液D.用装置丁蒸干MnCl2溶液制MnCl2·4H2O3−5.K3[Fe(CN)6]在水中可以电离出配离子[Fe(CN)6],下列关于该配离子的说法错误的是化学A.该配离子的中心离子为Fe3+B.该配离子的配体是CN−3−3+C.该配离子的配位数为6D.[Fe(CN)6]和Fe的性质相同22本卷满分100分,考试时间75分钟。6.在强碱中氢氧化铁可被一些氧化剂氧化为高铁酸根离子(FeO4),FeO4在酸性条件下氧化性极强且不稳定。注意事项:高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水处理剂,在水处理过程中,高铁酸钾转化为Fe(OH)3胶1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。体,制备高铁酸钾的流程如图所示。下列叙述错误的是2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。3.考试结束后,将本试卷和答题卡一并交回。______________________可能用到的相对原子质量:H1B11C12N14O16Na23S32V51Cu64As75一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要考号:A.铁屑在干燥的氯气中发生反应Ⅰ时,若铁屑过量,可能生成FeCl2求的。B.反应Ⅱ中氧化剂和还原剂的物质的量之比为3∶21.中国画中以墨色为主,以丹青色彩为辅,这样的水墨丹青画一般画在绢或纸上。下列说法错误的是C.该条件下,物质的溶解性:Na2FeO4KFeO24A.常见绢和纸的主要成分都是纤维素,纤维素属于天然高分子D.用KFeO对饮用水杀菌消毒的同时,生成的Fe(OH)胶体可吸附杂质净化水B.丹指朱砂,是HgS的天然矿石243_______________C.青指石青,主要成分为Cu(CO)(OH),该物质属于盐7.铑的配合物离子RhCOI可催化甲醇羰基化,反应过程如图所示。332222D.墨通过砚用水研磨可以产生用于毛笔书写的墨汁,墨汁属于胶体班级:2.下列化学用语正确的是A.乙醛的分子式:CH3CHOB.二氧化碳的空间填充模型:.丁烯的键线式:.基态氮原子的价电子排布图:_____________C2-D3.N为阿伏加德罗常数的值。下列说法正确的是A姓名:A.标准状况下,2.24LSO3含有的分子数为0.1NAB.60gNaHSO4晶体中含有的离子数为1.5NAC.0.5molC3H8中含有的共价键数为5.5NAD.3.9gNa2O2与足量水反应,转移的电子数为0.05NA______________4.氯气可用来制备将氢氧化铁氧化为高铁酸根离子的氧化剂,下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是学校:下列叙述错误的是A.CH3COI是反应中间体B.甲醇羰基化反应为CH3OH+COCH3CO2HC.反应过程中Rh的成键数目保持不变…D.上述过程中存在反应CH3OH+HICH3I+H2O化学试题第1页(共8页)化学试题第2页(共8页)………………○………………外………………○………………装………………○………………订………………○………………线………………○………………………………○………………内………………○………………装………………○………………订………………○………………线………………○………………………………………………………○……………………………………○……………………………线……………………○…………装………………○………………订……○………………………………………外………………○………○……………………………………………………○……线………………………………○………………………线……订………………○……………○……………………装……………………○……………○………………内…………8.山奈酚是中药柴胡的药物成分之一,结构如图所示。下列有关山奈酚的叙述正确的是下列说法正确的是A.T1K下,该反应进行40min时,2v正(NO2)=v逆(CO2)−1−1B.T1K下,前20min内NO2的降解速率为0.0125mol·L·minC.T2K下,若容器内气体平均摩尔质量不变,则反应处于平衡状态D.该反应在高温下才能自发进行A.该物质属于芳香烃B.分子中所有碳原子一定共平面12.W、X、Y、Z、Q是核电荷数依次增大的五种短周期元素。W的半径在所有离子中最小,X、Y、Z同C.不能使溴水和酸性KMnO4溶液褪色D.1mol山奈酚最多与3molNaOH反应周期且相邻,、位于同一主族且的核电荷数是的一半。下列说法正确的是ZQZQ封密不订装只卷此9.砷化硼晶体是具有超高热导率的半导体材料,其立方晶胞结构如图所示,若晶胞参数为anm。下列说法正A.Z、Q元素的最高正价相同确的是B.W、X、Y、Z四种元素不能形成离子化合物C.X、Q的最高价氧化物对应水化物的酸性:QXD.X、Y、Z分别与W形成的简单化合物的沸点:XYZ13.氯乙醇是一种重要的工业原料,可由乙烯经电解制备,其电解原理如图所示。下列说法正确的是A.砷化硼的化学式为B7As4B.与顶点B原子距离最近的B原子有6个3C.B、As原子之间的最短距离为anm43443D.该晶体的密度为3gcmNAa10.室温下进行下列实验,根据实验操作和现象所得到的结论正确的是A.a端电势高于b端电势实验操作和现象结论−B.理论上转移1mole,消耗28gCH2=CH2向X溶液中滴加几滴新制氯水,振荡,再加入少量2C.应选用阳离子交换膜,电解后电极室A中KOH溶液的浓度下降AX溶液中一定含有FeKSCN溶液,溶液变为红色+D.电极B上的电极反应式:Cl+H2O2e=HClO+H向3mLKI溶液中滴加几滴溴水,振荡,再滴加1mL淀−1−12+14.常温下,向10mL0.10mol·LCuCl2溶液中滴加0.10mol·LNa2S溶液,滴加过程中−lgc(Cu)与Na2S溶液BBr2的氧化性比I2的强粉溶液,溶液显蓝色−24−50体积(V)的关系如图所示。已知:常温下,Ksp(ZnS)=1.6×10;Ksp(Ag2S)=6.4×10。下列说法错误的是C向苯酚浊液中加入少量Na2CO3固体,浊液变清苯酚的酸性强于H2CO3的酸性pHCHCOONapHNaNO用试纸测得3溶液的约为9,2HNO2电离出H的能力比CH3COOHD溶液的pH约为8的强11.利用CH4消除NO2污染,反应原理为CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(g)。在1L密闭容器中,分别加入0.50molCH4和1.20molNO2,测得不同温度下n(CH4)(单位:mol)随时间变化的有关实验数据如表所示。A.c点溶液中:c(Na+)>c(Cl−)>c(S2−)>c(H+)时间/min组别温度/K物质的量/molB.相同条件下,若用等浓度等体积的ZnCl2溶液代替上述CuCl2溶液,则反应终点b向e的方向移动010204050C.a、b、c三点对应的溶液中,水的电离程度最大的为b点−1+2+−1①T1n(CH4)0.500.350.250.100.10D.向10mL物质的量浓度均为0.1mol·L的Ag、Cu混合溶液中逐滴加入0.01mol·L的Na2S溶液,+②T2n(CH4)0.500.300.18M0.15Ag先沉淀化学试题第3页(共8页)化学试题第4页(共8页)二、非选择题:本题共4小题,共58分。16.(15分)硫酸镍广泛应用于电镀、电池等工业。现以红土镍矿(主要成分为NiO,含MgO、Al2O3、Fe2O3、115.(14分)三水合硝酸铜[Cu(NO3)23H2O,M242gmol]是一种重要的无机试剂,常用作搪瓷着色剂,FeOOH、Fe3O4、CuO、ZnO、SiO2等杂质)为原料制备硫酸镍,工艺流程如下:也用于镀铜、制氧化铜及农药等。回答下列问题:Ⅰ.三水合硝酸铜[Cu(NO3)23H2O]的制备。实验室常用废铜屑与稀硝酸反应制备硝酸铜溶液,过滤出剩余铜屑,再经蒸发浓缩、冷却结晶、过滤、乙醇洗涤后得到三水合硝酸铜晶体。(1)制备硝酸铜时发生反应的离子方程式为_______________________________________。(2)若废铜屑中含有杂质铁,则检验所得硝酸铜溶液中含有铁元素的方法为_________________________已知:①相关金属离子[c(Mn)0.1molL1]形成氢氧化物沉淀的pH范围如下:___________________________。233222Ⅱ.Cu(NO3)2溶液的配制。金属离子FeFeAlMgZnNi1(3)实验室里需要450mL0.1molLCu(NO3)2溶液。用三水合硝酸铜Cu(NO3)23H2O配制该溶液时,______________________开始沉淀时的pH6.31.83.48.96.26.9下列仪器不需要的是_________________________(填仪器名称)。完全沉淀时的pH考号:8.33.24.710.98.28.9②当离子完全沉淀时,c(Mn)105molL1。−36−24−24−19③Ksp(CuS)=6.3×10,Ksp(ZnS)=1.6×10,Ksp(NiS)=1.4×10,Ksp(FeS)=3.7×10。④硫酸镍晶体(NiSO46H2O)可溶于水,不溶于乙醇和乙醚,乙醚微溶于水。_______________⑤硫酸镍在水中的溶解度随温度变化的曲线如图所示。(4)所需三水合硝酸铜固体的质量为_____________g。班级:(5)配制过程中,下列操作将导致溶液浓度偏小的是___________(填标号)。A.加水定容时俯视刻度线B.容量瓶未干燥处理C.定容加水时超过刻度线后,立即吸出多余的水_____________D.溶液从烧杯转移到容量瓶中后没有洗涤烧杯姓名:Ⅲ.三水合硝酸铜Cu(NO)3HO热分解实验。322回答下列问题:(6)将24.2gCu(NO)3HO样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图322(1)为加快“酸溶”速率,可采取的措施有_______________________________________(任写一条)。“滤渣所示。在TT℃过程中有红棕色气体产生,反应的化学方程式为__________________________。122”的主要成分有S和_____________(填化学式)。继续升温至T3℃时生成的固体产物为_____________(填化学式)。(2)写出“氧化除杂”过程中加入HO涉及反应的离子方程式:__________________________________。______________22(3)“氧化除杂”中加入Ni(OH)2的作用是_______________________________________,溶液的pH应调学校:节为_____________6。(4)“萃取,除杂”后所得水相的“系列操作”包括________、__________、________、洗涤得到硫酸镍晶体。(5)洗涤晶体的过程中最好选择___________(填标号)进行洗涤。A.蒸馏水B.无水乙醇C.乙醚D.稀盐酸…化学试题第5页(共8页)化学试题第6页(共8页)………………○………………外………………○………………装………………○………………订………………○………………线………………○………………………………○………………内………………○………………装………………○………………订………………○………………线…………
你可能还喜欢
购买VIP会员享超值特权
VIP专享免费下载,付费文档最高省50%
免费下载
付费折扣
身份标识
文档工具
限时7.4元/月购买VIP
相关推荐
-
地理-2024届高三12月大联考考后强化卷(河北卷)(全解全析)
2023-12-11 23:48
 4页
4页 -
生物-2024届高三12月大联考考后强化卷(河北卷)(全解全析)
2023-12-11 23:48
 7页
7页 -
历史-2024届高三12月大联考考后强化卷(河北卷)(全解全析)
2023-12-11 23:48
 5页
5页 -
历史-2024届高三12月大联考考后强化卷(河北卷)(考试版)
2023-12-11 23:48
 3页
3页 -
生物-2024届高三12月大联考考后强化卷(河北卷)(考试版)
2023-12-11 23:48
 4页
4页 -
化学-2024届高三12月大联考考后强化卷(河北卷)(全解全析)
2023-12-11 23:48
 6页
6页 -
物理-2024届高三12月大联考考后强化卷(河北卷)(考试版)
2023-12-11 23:48
 4页
4页 -
数学-2024届高三12月大联考考后强化卷(新课标I卷)(考试版)
2023-12-11 23:48
 2页
2页


 U1
U1